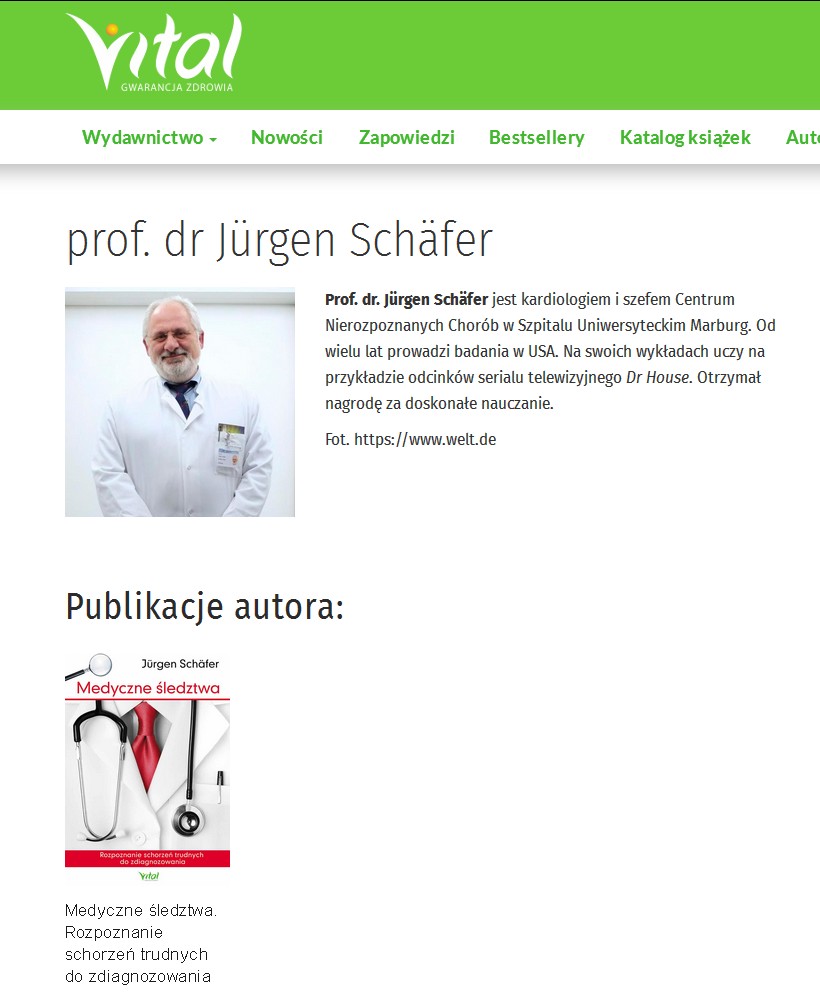
Do napisania tego artykułu zainspirowała mnie książka z 2015 r – autor prof. dr Jürgen Schäfer “”Medyczne śledztwa. Rozpoznanie schorzeń trudnych do zdiagnozowania.” Wydana z w 2017 przez “Vital. Gwarancja Zdrowia“
Lekarzy, którzy zajmują się trudnymi diagnostycznie, nierozpoznanymi (niezdiagnozowanymi) lub rzadkimi chorobami media lubią nazywać “Dr House” – od tytułowej postaci serialu o w/w tytule. Kojarzenie lekarza diagnosty z tą postacią może być pochlebne, ale prowadzi często do nieuzasadnionych nadziei pacjentów. Chory może myśleć, że ten lekarz jest jego “ostatnią deską ratunku” i on na pewno postawi właściwe rozpoznanie. Postać serialowego lekarza może także kojarzyć się z lekarzami pozbawionymi empatii dla pacjenta, dla których ważniejsze jest rozpoznanie niż sam chory. Serialowy “Dr House” miał 100% skuteczność w odkrywaniu prawdziwych rozpoznań. Osiągał to dzięki dużym umiejętnościom detektywistycznym w stylu Sherlocka Holmesa, wspaniałemu zespołowi współpracowników i najnowocześniejszemu sprzętowi diagnostycznemu oraz nowoczesnym medycznym bazom danych. Stawiał on także rozpoznania “ex iuvantibus“, często ryzykując życie pacjentów w niecierpiących zwłoki (tzw. “urgensowych”) sytuacjach.
W prawdziwym świecie tak łatwo nie jest. Samych chorób rzadkich jest ponad 8 tysięcy. Rodzajów patogenów są miliony. Takie same objawy kliniczne mogą występować w kilku różnych jednostkach chorobowych równocześnie. Ponadto pacjent może mieć kilka chorób na raz (np. jeden stosunek płciowy może. Istnieje ), gdzie jest tyle zmiennych środowiskowych, genetycznych, zawodowych, osobniczych – żaden lekarz nie jest w stanie zagwarantować pacjentowi, że na pewno postawi prawdziwe rozpoznanie. Pacjenci czasem świadomie lub nie utrudniają proces diagnostyczny (Dr House miał zasadę -Wszyscy kłamią). Często istnieje olbrzymia walka z czasem (widzieliśmy to w serialu), brak pieniędzy na badania, brak dostępu do sprzętu i konsultantów. Także pacjent nie zawsze wytrzymuje zdrowotnie, finansowo i psychicznie ilość i rodzaj zleconych badań. (Nie raz obserwowałem to w swojej praktyce). Czasem trzeba wybierać mniejsze zło i odstępować od badań, które przyniosą więcej szkody niż pożytku choremu (pacjent umrze na skutek powikłań diagnostycznych a nie na chorobę, której szukamy).
Dlatego też odpowiedzialny lekarz, woli się nazywać lekarzem od niezdiagnozowanych (nierozpoznanych) (trudnych diagnostycznie przypadków chorobowych) oraz chorób rzadkich – to daje uczciwy obraz procesu diagnostycznego i nie rodzi fałszywych nadziei. Prof. Gahl (USA) zakłada, że sukcesem będzie jeśli postawi rozpoznanie u 10-15% swoich wyselekcjonowanych pacjentów z nierozpoznanymi chorobami.
Nie zwalnia to nas z uczciwej i benedyktyńskiej ciężkiej pracy, która nie zawsze kończy się sukcesem. W procesie diagnostycznym liczy się wytrwałość i upór lekarza ( jak w polskim filmie :Kiler” -“Masz być jak bulterier” 🙂 ), ale także pacjenta i jego rodziny.
Prawdą jest, że serial “Dr House” pokazuje, iż nie można się poddawać w dążeniu do prawidłowego rozpoznania, zainspirował wielu lekarzy do wnikliwszej analizy przypadków chorobowych, spojrzenia niekonwencjonalnego (innego niż poprzednicy) na objawy pacjenta, pokazał rzadkie przypadki chorobowe (były one podpowiedziom dla lekarzy w kontakcie z prawdziwymi przypadkami z ich własnej praktyki, stanowił także świetny materiał dydaktyczny do nauczania studentów medycyny. Profesor Jürgen Schäfer jest właśnie takim dydaktykiem, któremu niemieckie media przyznały tytuł “niemieckiego Doktora House’a”).
W Niemczech istnieje cała sieć ośrodków chorób rzadkich (powstają one także powoli w Polsce- Warszawa, Łódź, Gdańsk, Kraków), natomiast mało jest placówek zajmujących sie kompleksowo tzw. “Niezdiagnozowanymi” chorobami (jest to szersze pojecie niż choroby rzadkie. Nie ma co ukrywać, taka placówka może pociągnąć finansowo na dno nie jeden szpital ze względu na wysoki koszt diagnozowania i leczenia jednego pacjenta. Bardziej opłaca się leczyć 100 prostych przypadków niż prowadzić trudną diagnostykę jednego pacjenta.
W USA pracuje prof. dr William A. Gahl , który zajmuje się także niezdiagnozowanymi przypadkami. Włożył on duży wkład w integrację środowiska medycznego w rozpoznawaniu chorób niezdiagnozowanych
Niemiecki “dr House” prof. dr Jürgen Schäfer

Centrum Chorób Nieznanych (niezdiagnozowanych) i Rzadkich
ZusE
adres:
Zentrum für unerkannte und seltene Erkrankungen
Universitätsklinikum Gießen – Marburg
Standort Marburg
Baldingerstraße 1
35043 Marburg
Mail: zuse@uk-gm.de
Tel. 06421-586 4357
Fax. 06421-586 4857
Polecane linki w książce Pana Profesora
https://www.patienten-information.de/checklisten
https://www.weisse-liste.de/de/service/fuer-aerzte/, https://www.aezq.de/,
Mittelhessenbotschafter Professor Schäfer spricht über Dr. House und
die Region (made by mediashots)
Der deutsche “Dr. House”: Professor Schäfer gewinnt Pulsus
https://www.youtube.com/watch?v=UejzOkCWqWk
(zatrucie kobaltem)
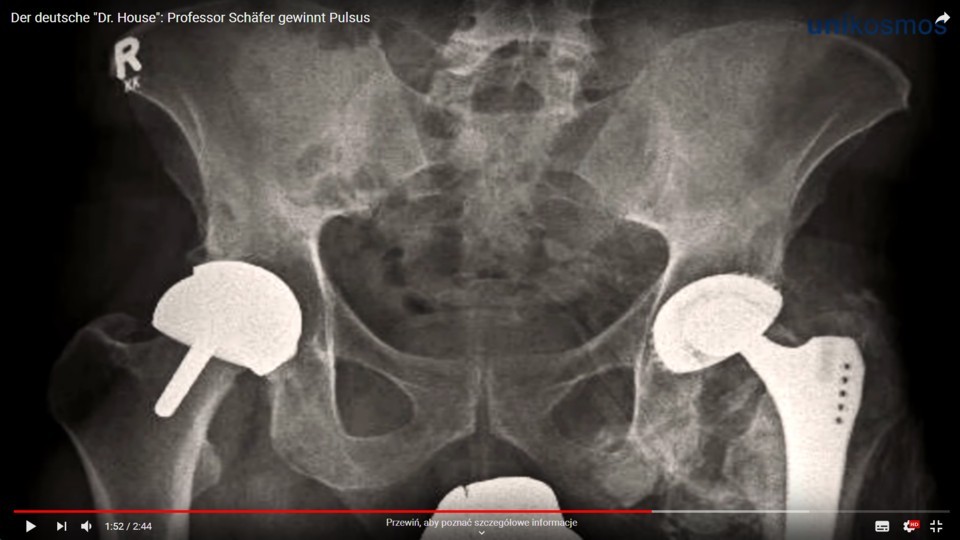
Zatrucie kobaltem
Prof. Schäfer osiągnął spektakularny sukces diagnostyczny. Naukowiec twierdzi, że zawdzięcza go właśnie serialowi Dr House (o czym napisał także w swojej książce). W jednym z odcinków filmu była mowa o zatruciu kobaltem u pacjenta, który miał uszkodzoną porcelanową (pokruszoną) protezę stawu biodrowego. Po wymianie protezy na metalową doszło do niszczenia metalu przez ocierające ją pozostałe w okolicy stawu odłamki porcelany i uwolnienia się kobaltu do organizmu. Stan chorego dramatycznie się pogorszył. Doszło do rozwoju kardiomiopatii – parametry ECHO (USG serca) kwalifikowały pacjenta do przeszczepu serca. Ustalenie zatrucia kobaltem, wymiana protezy pozwoliła choremu do pełnego powrotu do zdrowia. Profesor przekazał choremu nowinę, że nieistniejący Dr House pozwolił go wyleczyć 🙂 Dodajmy, że ustalenia tego rozpoznania, u pacjenta bez zawodowego narażenia na kobalt było dużą sztuką diagnostyczną. Lekarze zwykle nie spotykają się z takimi przypadkami w swojej. Metody diagnostyczne muszą być celowane (ale na to trzeba “wpaść”, aby je zlecić).
Panie Profesorze!
Wyrazy Szacunku i Uznania! Pana pasja dydaktyczna i wykorzystanie nowoczesnych technologii – uratowały życie chorego.


Der deutsche “Dr. House”: Professor Schäfer gewinnt Pulsus
http:// https://www.youtube.com/watch?v=UejzOkCWqWk
Diagnoza dr House’a uratowała pacjenta z tajemniczą chorobą(http://www.tvn24.pl) (7.02.
5 Fragen an den deutschen Dr. House
W tym filmie profesor mówi o narzędziach komputerowych wykorzystywanych w diagnostyce trudnych przypadków: Google Scholar, Uptodate, Isabel Healthcare, Orphanet, Medline (PubMed)
(Dzisiaj sam także korzystałem z tych baz dla mojej 5 letniej pacjentki – z narzędzi: phenomizer orhanet, oraz symptomchecker.isabelhealthcare )
IBM Watson und RHÖN-KLINIKUM AG
Wykorzystują także bazę danych IBM Watson
Profesor Schafer uważa, że naukowcy powinni zwracać większą uwagę na osoby, które nie zachorowały na daną chorobę z rodziny obciążonej czynnikami ryzyka (np. wada genetyczna), bo tam może tKwić klucz na rozwiązanie problemów członków rodziny
What to learn from rare diseases | Jürgen Schäfer | TEDxRWTHAachen
https://www.youtube.com/watch?v=5CdP7DHhWOM
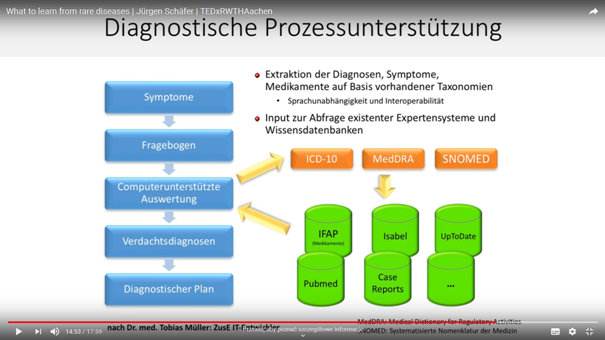
Profesor pokazuje duże koszty diagnostyki trudnych przypadków – np. zapalenie wsierdzia 8 tys Euro. Pod koniec wykładu (14 minuta) zdradza sekrety własnego warsztatu diagnostycznego – badanie przedmiotowe, formularze w pytaniami dla pacjenta (96 stron), komputerowe bazy danych (sytemy expertowe – Isabel Healtcare, PubMed, IFAP medicamente, UpToDate, Case raports,(inneJournal of Medical Case Reports, BMJ Case Reports, Clinical Case Reports )MedDRA, SNOMED, wykorzystuje numeracje ICD-10
Amerykański “Dr House” prof. dr William A. Gahl

prof. William Gahl – kierownik Kliniki Chorób Niezdiagnozowanych
National Institute of Health’s Undiagnosed Diseases Program
https://www.genome.gov/10005723/gahl–group/
Clinical Director of the National Human Genome Research Institute at the National Institues of Health, Rare and Undiagnosed Diseases Program.
Adres:
Building 10, Room 10C103
10 Center Drive
Bethesda, MD 20892, gahlw@helix.nih.gov, tel. 301-402-2739
Director Undiagnosed Diseases Program
Senior Investigator
Medical Genetics Branch
Head
Human Biochemical Genetics Section , ,
Genetic and Rare Diseases Information Center
Patienten ohne Diagnose: Wenn der echte Dr. House ermittelt
William Gahl – kierownik kliniki chorób niezdiagnozowanych
National Institute of Health’s Undiagnosed Diseases Program
Profesor Gahl wprowadza nowoczesne metody diagnostyczne i współpracuje z innymi ośrodkami zajmującymi się chorobami niezdiagnozowanymi (sieć UDN)
–
Undiagnosed Diseases Network w Wikipedii
National Institute of Health’s Undiagnosed Diseases Program
Autorzy filmu w wywiadzie z profesorem W. Gahl pokazują prace oddziału i między innymi przypadek Sally M., u której wykryto przyczynę nadmiernego rozrostu mięśni. Był to rzadki rak z komórek macierzystych szpiku (steam cells cancer). Leczenie z przeszczepem komórek macierzystych przyniosło poprawę.40% pacjentów to dzieci podejrzane o wadę genetyczną.
Medical Mysteries and Rare Diseases: William Gahl at TEDxCMU 201
Rare and Undiagnosed Disease Program: Mayo Clinic Radio
Wywiad w radio Mayo Clinic Opublikowany 13 lis 2017
Dr. William Gahl, Clinical Director of the National Human Genome Research Institute at the National Institues of Health, discusses the Rare and Undiagnosed Diseases Program. This interview originally aired Nov. 11, 2017.
Inni
Solving the mystery of rare diseases with technology and crowdfunding: Jimmy Lin at TEDxMidAtlantic
Jimmmy Lin pracuje w Rare Genomics Institute – wprowadzili crowdfunding w zbieraniu funduszy na diagnostykę i leczenie dzieci z chorobami rzadkimi.